Comportamiento de los coloides
Propiedades eléctricas
Aquí entramos en la descripción del comportamiento de superficies
cargadas eléctricamente. Una gran parte del material se basa en
estudios electroquímicos, por lo cual sería recomendable
que el lector desempolvara sus conocimientos referentes a electrodos y
diferencias de potencial electroquímico. Mucho de lo que se ha descubierto
con respecto al comportamiento de superficies de electrodos puede aplicarse
al estudio de interfases entre partículas coloidales y el medio
dispersante.
Modos en que una superficie puede adquirir carga
Existen varios mecanismos mediante los cuales una superficie puede adquirir
carga. Entre ellos están:
-
Ionización de grupos superficiales
-
Disolución diferencial
-
Sustitución isomórfica
-
Superficies cristalinas cargadas
Los nombres son bastante explícitos, pero conviene elaborar un poco
acerca de algunos de ellos: la ionización de grupos superficiales
sucede con mucha frecuencia en biomoléculas. En el caso de proteínas,
éstas poseen grupos cuyo estado de ionización depende del
pH, como son los grupos carboxilo y amino. A pH bajo, los grupos carboxilo
estarán protonados y los grupos amino también, lo cual dotará
a la superficie de la proteína con una carga positiva. Si el pH
es alto, la carga será negativa debido a que los grupos amino estarán
en la forma de base libre, mientras que los grupos ácidos estarán
en la forma de carboxilato. Esto significa que a un cierto pH, en principio,
se puede inducir electroneutralidad, balanceando el número de grupos
ácidos y básicos. A este punto se le llama el punto
isoeléctrico de una proteína. Por razones que estudiaremos
más tarde, en este punto se logra más fácilmente que
precipiten muchas proteínas.
La disolución diferencial es análoga a la ionización
de grupos superficiales en que depende de la función p de un ion.
Por ejemplo, en el caso del AgI, el cual es una sal muy insoluble en agua,
la carga sobre la superficie de las partículas formadas depende
del ion más abundante. Si añadiéramos NaI, podríamos
controlar la carga de las partículas controlando el pI. Del mismo
modo que en el caso de las proteínas, sería posible alcanzar
un análogo del punto isoeléctrico.
La sustitucón isomórfica se da cuando existe un ion espectador
en la solución, y éste ion puede incorporarse a la red cristalina
del sólido formado. Si el ion espectador tiene una carga diferente
a la de los iones de la red cristalina, el exceso (o defecto) de carga
dotará a la superficie de una carga negativa (o positiva).
Retomando el concepto de índices de Miller, vemos que diferentes
caras de una celda unidad poseen diferentes abundancias de los iones que
la constituyen (si los índices de Miller son diferentes). Esto resulta
en que diferentes caras de la celda unidad posean diferentes cargas.
Potencial eléctrico en una interfase
Ver sección 11.4 del libro de Atkins
Teorías de la doble capa eléctrica
Mucho de lo que se sabe acerca de la doble capa eléctrica se ha
aprendido mediante estudios electroquímicos. De hecho, Heyrovsky,
el gran electroquímico checo, inventó el electrodo de gota
de mercurio --que luego se adoptó para polarografía-- para
hacer estudios de interfases cargadas, incluyendo mediciones de tensión
superficial.
Helmholtz
Cuando una superficie posee una carga neta, esta carga ejercerá
una atracción coulómbica neta sobre los contraiones que se
encuentren en las cercanías. Helmholtz postuló la formación
de una doble capa eléctrica, esto es, de dos capas adyacentes con
cargas opuestas. Este modelo incluye varias suposiciones:
-
Las cargas son puntuales
-
Las cargas están fijas en sus posiciones
-
La carga reside exclusivamente en la superficie (tanto la carga de la partícula
como los contraiones)
A este modelo también se le llama de la doble capa compacta.
Este modelo, por lo tanto, describe la superficie de una partícula
como un capacitor de placas paralelas. El modelo de Helmholtz postula
una capacitancia constante. Es posible medir la capacitancia de la
superficie de partículas coloidales, pero los experimentos indican
que la capacitancia no es constante.
Gouy-Chapman
El modelo de Gouy-Chapman es una modificación del modelo de Helmholtz.
Todavía postula cargas puntuales, pero toma en cuenta el movimiento
debido a agitación térmica, por lo que postula una doble
capa difusa, esto es, la carga de la partícula reside en la
superficie, pero los contraiones no están fijos en la superficie
sino que se mueven continuamente. Esto requiere el postulado adicional
de una distribución de Bolzmann para describir la abundancia de
partículas a una distancia d de la superficie. El que
la distribución de partículas siga una distribución
de Bolzmann significa, de modo simplificado, que el potencial eléctrico
en la solución que rodea a la superficie decae exponencialmente
con la distancia a la superficie. Este modelo postula una capacitancia
variable, y corresponde cualitativamente a las mediciones experimentales.
Al grosor de la doble capa eléctrica se le llama longitud de
Debye.
Gouy-Chapman-Stern
Stern añadió otra modificación al modelo de Gouy-Chapman:
consideró que los contraiones no son partículas puntuales,
sino que poseen un tamaño finito. Por esta razón, la
carga (la cual se considera localizada en el centro de la partícula,
de modo que toda la superficie posee una carga uniforme) no puede acercarse
a una distancia arbitrariamente pequeña, sino sólo hasta
una distancia igual al radio del contraion. A esta distancia mínima
de aproximación se le llama capa de Stern. Normalmente
se considera a la capa de Stern como equivalente a la superficie cortante,
esto es a la superficie de la capa que se encuentra en "contacto directo"
con la masa de la fase dispersante.
Cálculo del potencial zeta
Al potencial eléctrico sobre la superficie cortante se le llama
potencial electrocinético o potencial zeta y se considera igual
al potencial sobre la capa de Stern. Por lo general, esta suposición
introduce solamente errores pequeños. Para caracterizar la
partícula de la cual se quiere calcular el potencial zeta, se usa
el cociente del radio de la partícula, k, y el espesor de
la doble capa, a; k/a. Este parámetro normalmente se
abrevia como ka
Ecuación de Hückel para ka pequeño
Esta ecuación se usa cuando se considera una carga puntual
y por lo tanto ka es muy pequeño:
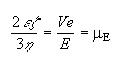
Ecuación de Smoluchovski
Se usa cuando las partículas tienen tamaño finito, por lo
que ka tiene un valor apreciable:
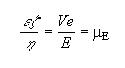
Ahora tenemos el problema de decidir cuándo usar cada una de
las ecuaciones. Aquí viene Henry al rescate.
Ecuación de Henry
Henry propuso una ecuación más general que la de Hückel
o la de Smoluchovski:
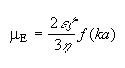 donde f(ka) es una función numérica de la siguiente forma
aproximada:
donde f(ka) es una función numérica de la siguiente forma
aproximada:
Problemas de la ecuación de Henry:
-
Conductancia superficial: la distribución de iones en la doble capa
eléctrica produce conductancia, lo cual distorsiona el campo eléctrico.
Si ka es grande se subestima el potencial zeta.
-
Relajación: Cuando la partícula se mueve, distorsiona la
doble capa. Esta atmósfera iónica asimétrica
retarda el movimiento de la partícula.
Propiedades electrocinéticas
La presencia de cargas en la superficie de las partículas coloidales
las hace sensibles a diferencias de potencial aplicadas y hace que sean
capaces de inducir diferencias de potencial cuando se mueven. Estas
manifestaciones se agrupan dentro de las propiedades electrocinéticas.
La siguiente tabla resume las relaciones entre las diversas propiedades
electrocinéticas, ya sea que respondan a una diferencia de potencial
o la induzcan, o que la superficie sea estacionaria o móvil.
| Diferencia de potencial |
Superficie estacionaria |
Superficie móvil |
| Aplicada |
Electroósmosis |
Electroforesis |
| Inducida |
Potencial de flujo |
Potencial de sedimentación |
Electroósmosis y potencial de flujo
Electroósmosis: movimiento de líquido respecto a una superficie
cargada estacionaria cuando se aplica una diferencia de potencial
Potencial de flujo: diferencia de potencial que aparece cuando un líquido
fluye a lo largo de una superficie cargada estacionaria.
Electroforesis y potencial de sedimentación
Electroforesis: movimiento de partículas cargadas respecto
a un líquido estacionario cuando se aplica una diferencia de potencial.
La electroforesis consiste en la migración de partículas
de tamaño coloidal que poseen carga neta a través de una
solución, cuando se somete ésta a la influencia de una corriente
eléctrica. Este método fue descubierto en 1807 por
Reus y a la fecha está muy difundido para separación e caracterización
de proteínas y otras biomoléculas. Existe una variedad
de técnicas de electroforesis, entre otras:
-
Electroforesis de límite móvil
-
Electroforesis de zona
-
Electroforesis de disco
-
Electroforesis de cortina
Electroforesis de límite móvil
Como se ve en el diagrama, uno de los brazos y la parte inferior del tubo
en forma de U se llenan con solución de muestra y el otro brazo
se llena con una solución reguladora de pH. Entonces se forma
un límite bien marcado entre las dos soluciones. Los electrodos
se sumergen en una solución reguladora y todo el aparato se equilibra
a 4°C, para reducir las corrientes de convección producidas
por el calor de la corriente eléctrica.
Al hacer pasar una corriente eléctrica a través de la
celda, cada componente se mueve a una velocidad dependiente de la magnitud
de su carga eléctrica y de su forma. Esto se manifiesta como
varios límites móviles. Para detectar los límites
móviles se utiliza óptica Schlieren. Para obtener el
patrón de electroforesis, se grafica el gradiente de índice
de refracción contra la distancia a lo largo del tubo. La
movilidad electroforética de cada especie es una propiedad característica
y se puede calcular con la siguiente ecuación:
(mu) = dAK/it
donde
-
d
-
distancia que el límite se desplaza en el tiempo t
-
t
-
tiempo
-
A
-
área de la sección transversal del tubo
-
K
-
conductividad de la solución reguladora
-
i
-
corriente aplicada
Electroforesis de zona
En la electroforesis de zona, las sustancias se colocan sobre un soporte
sólido, en lugar de estar en solución. Los soportes
más comunes son geles de almidón, geles de poliacrilamida,
espuma de poliuretano y papel. Los geles de poliacrilamida reducen
mucho las interferencias debidas a convección y difusión,
aunque los geles de alimidón todavía se emplean ampliamente.
Después de preparar una placa de gel, la muestra se coloca en una
línea angosta en el centro de modo que los componentes puedan migrar
hacia los lados.
Es común que la placa posea un gradiente de pH, de este modo,
las proteínas migran hasta la región en la que alcanzan su
punto isoeléctrico.
Electroforesis de disco
Es similar a la cromatografía de exclusión o de permeación
en gel: las proteínas descienden en bandas delgadas (o discos) a
través de un gel que se mantiene a pH constante. Puede impregnarse
el gel con un colorante para revelar la posición de las bandas.
Es útil para separar ácidos nucleicos.
Electroforesis de cortina
En este caso el soporte es una hoja de papel, la parte superior del papel
se encuentra sumergida en un solvente que ayuda a la elución mientras
la muestra se aplica continuamente mediante un filamento también
en la parte superior del papel. Los componentes bajan por la acción
de la gravedad y lo hacen a distintas velocidades. Además
las muestras están sometidas a un campo eléctrico que hace
que los componentes se separen por carga. Una molécula sin
carga bajará en línea recta.
Potencial de sedimentación: diferencia de potencial que
aparece cuando partículas cargadas se mueven en un líquido
estacionario.
Tema siguiente
Tema anterior
Vuelta al temario
Ultima actualización de esta página: 7 de agosto de 1998
Encargado de la página: Dr. Víctor Manuel Rosas García.
e-mail:vrosas@ccr.dsi.uanl.mx
Facultad de Ciencias Químicas
Universidad Autónoma de Nuevo León
San Nicolás de los Garza, NL, México.